
醫(yī)療器械產(chǎn)品出口銷售證明
醫(yī)療器械產(chǎn)品出口銷售證明
醫(yī)療器械產(chǎn)品出口銷售證明

1、在本市已取得醫(yī)療器械產(chǎn)品注冊證書及生產(chǎn)許可證書,或已辦理醫(yī)療器械產(chǎn)品備案及生產(chǎn)備案的,上海市食品藥品監(jiān)督管理局可為相關(guān)生產(chǎn)企業(yè)出具《醫(yī)療器械產(chǎn)品出口銷售證明》。
2、需要出具《醫(yī)療器械產(chǎn)品出口銷售證明》的企業(yè),其生產(chǎn)不符合相關(guān)法規(guī)要求,企業(yè)信用等級較低,或在生產(chǎn)整改、涉案處理期間的,不予出具《醫(yī)療器械產(chǎn)品出口銷售證明》。
3、企業(yè)應(yīng)當(dāng)**所出口產(chǎn)品符合醫(yī)療器械出口相關(guān)規(guī)定要求,并應(yīng)當(dāng)符合進口國的相關(guān)要求,且已經(jīng)辦理了生產(chǎn)出口醫(yī)療器械備案,在出口過程中所發(fā)生的一切法律責(zé)任,由企業(yè)自行承擔(dān)。
4、企業(yè)提交的相關(guān)資料發(fā)生變化的,應(yīng)當(dāng)及時報告出具證明部門。相關(guān)資料發(fā)生變化或有效期屆滿仍需繼續(xù)使用的,企業(yè)應(yīng)當(dāng)重新辦理《醫(yī)療器械產(chǎn)品出口銷售證明》。
5、企業(yè)提供虛假證明或者采取其他欺騙手段騙取《醫(yī)療器械產(chǎn)品出口銷售證明》的,5年內(nèi)不再為其出具《醫(yī)療器械產(chǎn)品出口銷售證明》,并將企業(yè)名稱、醫(yī)療器械生產(chǎn)許可證或備案憑證編號、醫(yī)療器械產(chǎn)品注冊證或備案憑證編號、法定代表人和組織機構(gòu)代碼等信息予以通告。
醫(yī)療器械產(chǎn)品出口銷售證明出具的審查實行書面材料和網(wǎng)上信息雙軌制審查形式。受理部門收到辦事申請后,應(yīng)按照下列要求,當(dāng)場對企業(yè)提交材料的完整性進行核對,填寫上海市出具醫(yī)療器械產(chǎn)品出口銷售證明申請資料一覽表。
(1)企業(yè)應(yīng)按照"七、(二)行政審批申請材料目錄"的要求提交全部申請材料,申請材料應(yīng)清晰、可辨認;
(2)對照網(wǎng)上申請信息和紙質(zhì)材料,兩者應(yīng)一致;
(3)對照申請信息與醫(yī)療器械生產(chǎn)許可證,其中企業(yè)名稱、法定代表人、企業(yè)負責(zé)人、住所地址應(yīng)與醫(yī)療器械生產(chǎn)許可證內(nèi)容一致(第二、三類醫(yī)療器械生產(chǎn)企業(yè)適用)或者應(yīng)與第一類醫(yī)療器械生產(chǎn)備案憑證的內(nèi)容一致(第一類醫(yī)療器械生產(chǎn)企業(yè)適用);
(4)在上海市食品藥品監(jiān)督管理局行政審批平臺(http://xuke.smda.gov.cn)中查詢擬申請出具出口銷售證明的醫(yī)療器械產(chǎn)品的生產(chǎn)出口醫(yī)療器械備案記錄,應(yīng)已完成生產(chǎn)出口醫(yī)療器械備案;
(5)備案材料應(yīng)附有目錄,排列有序,裝訂整齊,逐頁編碼,頁號用阿拉伯?dāng)?shù)字編寫在頁面底部,紙張無破損、規(guī)格統(tǒng)一(一般用A4紙);
(6)復(fù)印件應(yīng)注明"與原件核對無誤",并加蓋公章;
(7)卷內(nèi)文字應(yīng)使用藍黑、碳素墨水鋼筆或者簽字筆。
營業(yè)執(zhí)照、組織機構(gòu)代碼證、醫(yī)療器械的注冊證或者備案憑證等復(fù)印件加蓋公章后與電子版一并留存,并根據(jù)下列情況分別作出處理:
(1)符合形式標(biāo)準(zhǔn)的予以受理,并發(fā)給受理通知書(一式兩份,一份交企業(yè)申請人,另一份放入申請資料),并加業(yè)務(wù)受理專用章。
(2)對于缺少規(guī)定的資料、資料的內(nèi)容不完整、資料中有明顯錯誤、未完成網(wǎng)上信息填報的或網(wǎng)上信息與書面材料不一致的,應(yīng)要求企業(yè)改正。對于可以當(dāng)場改正的內(nèi)容,允許企業(yè)當(dāng)場改正,并簽署委托辦理人的姓名和日期。對于無法當(dāng)場改正的,受理部門告知企業(yè)補正材料。
(3)申請事項不屬于本部門職權(quán)范圍的或不符合申請條件的,可當(dāng)場作出不予受理的決定。
根據(jù)《醫(yī)療器械產(chǎn)品出口銷售證明登記表》上提供的信息與企業(yè)提供的申請資料核對,對申請生產(chǎn)企業(yè)的資質(zhì)進行審核,完成《醫(yī)療器械產(chǎn)品出口銷售證明》證書的譯制。《醫(yī)療器械產(chǎn)品出口銷售證明》編號的編排方式為:滬食藥監(jiān)械出XXXXXXXX號。其中:第一位X到第四位X代表4位數(shù)的證明出具年份;第五到第八位X代表4位數(shù)的證明出具流水號。《醫(yī)療器械產(chǎn)品出口銷售證明》有效日期不應(yīng)超過申報資料中企業(yè)提交的各類證件**到達的截止日期,且*長不超過2年。完成證書的譯制后,提交行政復(fù)核。
根據(jù)譯制完成的《醫(yī)療器械產(chǎn)品出口銷售證明》與企業(yè)申請資料進行復(fù)核,做出是否予以出具的決定。
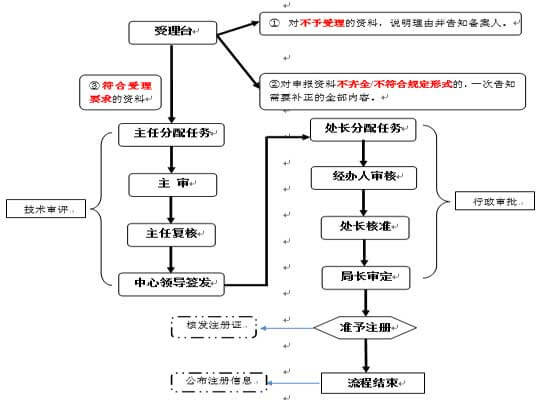
醫(yī)療設(shè)備出口辦理流程
1、準(zhǔn)備文件(包括CE證書,文件,企業(yè)信息等)
2、由歐代將資料提交到EEA各成員國主管機關(guān)(英國為DH)
3、簽發(fā)證書
4、進行使館公證
相當(dāng)于自由銷售證明,一般是目的國藥監(jiān)局要求的,只有把需要出口產(chǎn)品在目的國藥監(jiān)部門注冊之后,才被允許在進口國銷售。這個醫(yī)療器械產(chǎn)品出口銷售證明,是一個在目的國注冊必須的文件。 如果不提供這個文件,即使你通過了出口國和進口國的海關(guān),客戶也沒辦法在當(dāng)?shù)厥袌龊戏ㄤN售。
1、準(zhǔn)備文件(包括CE證書,文件,企業(yè)信息等)
2、由歐代將資料提交到EEA各成員國主管機關(guān)(英國為DH)
3、簽發(fā)證書
4、進行使館公證
【答】辦理出口證明書免費。但是分兩種,國內(nèi)注冊過的和沒注冊過的。辦理注冊證的費用(免除人工費用和接待費用,免除咨詢費用),檢測費2萬以內(nèi),臨床費用15萬以內(nèi)。GMP費用得看生產(chǎn)的產(chǎn)品,如果是無菌產(chǎn)品那費用可大了去了。沒經(jīng)驗的咨詢費用在5萬。
【答】在國家食品藥品監(jiān)督管理局(SFDAS)網(wǎng)站下載"醫(yī)療器械(體外診斷試劑)電子申報軟件",填寫出口申請表。
1、醫(yī)療器械產(chǎn)品出口銷售證明書依據(jù)產(chǎn)品是否已取得醫(yī)療器械注冊證分為兩種格式。 對于已取得醫(yī)療器械注冊證的產(chǎn)品,其出口銷售證明書的主要內(nèi)容為:產(chǎn)品符合中華人民共和國有關(guān)標(biāo)準(zhǔn),已在中國注冊,準(zhǔn)許在中國市場銷售,出口不受限制。 對于未取得醫(yī)療器械產(chǎn)品注冊證的產(chǎn)品,其出口銷售證明書的主要內(nèi)容為:產(chǎn)品未在中國注冊,尚未進入中國市場,但出口不受限制。
2、醫(yī)療器械出口銷售證明書的有效期為2年。
3、醫(yī)療器械產(chǎn)品出口銷售證明書的申請者可以是生產(chǎn)企業(yè)或出口企業(yè)。
4、已取得醫(yī)療器械注冊證的產(chǎn)品,申請醫(yī)療器械產(chǎn)品出口銷售證明書,應(yīng)填寫申請表,并提交下列文件:
1)所出口產(chǎn)品生產(chǎn)者的《醫(yī)療器械生產(chǎn)企業(yè)許可證》(復(fù)印件)
2)所出口產(chǎn)品的《醫(yī)療器械注冊證》(復(fù)印件)
3)出口企業(yè)的營業(yè)執(zhí)照(復(fù)印件)
4)申請者的自我**聲明,**所出口產(chǎn)品滿足藥品監(jiān)督管理部門對該產(chǎn)品生產(chǎn)和注冊的法規(guī)要求,所提交的材料真實合法。
5、未取得醫(yī)療器械產(chǎn)品注冊證的產(chǎn)品,申請醫(yī)療器械產(chǎn)品出口銷售證明書,應(yīng)填寫申請表(格式見附件3),并提交下列文件:
1)生產(chǎn)企業(yè)的營業(yè)執(zhí)照(復(fù)印件)
2)出口企業(yè)的營業(yè)執(zhí)照(復(fù)印件)
3)申請者自我**聲明,**所提交的材料真實合法。
所提交的證書復(fù)印件需加蓋證書所屬企業(yè)公章。
6、醫(yī)療出口企業(yè)應(yīng)**所出口產(chǎn)品符合出口要求,在出口過程中所發(fā)生的一切法律責(zé)任,由出口企業(yè)自行承擔(dān)。
7、醫(yī)療器械產(chǎn)品出口銷售證明書的工作時限為15個工作日。
8、本規(guī)定自發(fā)布之日起施行。