《體外診斷試劑注冊(cè)管理辦法》所稱的體外診斷試劑,是指按醫(yī)療器械管理的體外診斷試劑,包括在疾病的預(yù)測(cè)、預(yù)防、診斷、治療監(jiān)測(cè)、預(yù)后觀察和健康狀態(tài)評(píng)價(jià)的過(guò)程中,用于人體樣本體外檢測(cè)的試劑、試劑盒、校準(zhǔn)品、質(zhì)控品等產(chǎn)品。可以單獨(dú)使用,也可以與儀器、器具、設(shè)備或者系統(tǒng)組合使用。
《體外診斷試劑注冊(cè)管理辦法》所稱的體外診斷試劑,是指按醫(yī)療器械管理的體外診斷試劑,包括在疾病的預(yù)測(cè)、預(yù)防、診斷、治療監(jiān)測(cè)、預(yù)后觀察和健康狀態(tài)評(píng)價(jià)的過(guò)程中,用于人體樣本體外檢測(cè)的試劑、試劑盒、校準(zhǔn)品、質(zhì)控品等產(chǎn)品。可以單獨(dú)使用,也可以與儀器、器具、設(shè)備或者系統(tǒng)組合使用。
免費(fèi)
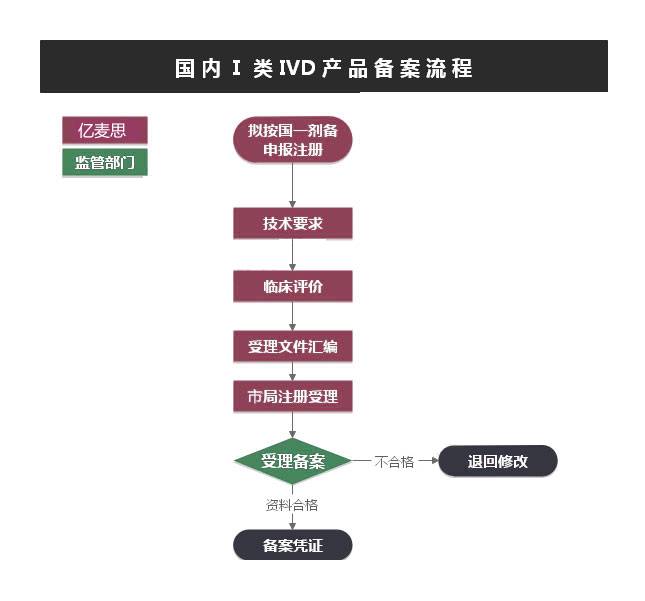
立項(xiàng)階段
預(yù)算、合同、考慮期,0.5個(gè)月。
申報(bào)前資料準(zhǔn)備
資料提供
產(chǎn)品技術(shù)要求編制
產(chǎn)品自測(cè)/委托檢測(cè)
產(chǎn)品備案資料編寫(含臨床評(píng)價(jià)資料)
2-3個(gè)月
申報(bào)后
產(chǎn)品備案受理,備案憑證 1天
*補(bǔ)正資料:若資料不齊全,須補(bǔ)正后再受理
預(yù)算合計(jì)
4個(gè)月
I類IVD NMPA國(guó)內(nèi)產(chǎn)品備案服務(wù)
I類IVD NMPA國(guó)內(nèi)臨床評(píng)價(jià)資料撰寫服務(wù)
I類IVD NMPA國(guó)內(nèi)醫(yī)療器械生產(chǎn)備案咨詢服務(wù)
I類IVD NMPA生產(chǎn)備案咨詢服務(wù)